产品搜索
结构搜索
全站搜索
当前位置: 专题聚焦
直面病毒,不惧前行|丙型肝炎病毒特点及其检测进展
本文转自医学界感染频道
丙型肝炎-沉默的杀手
丙型肝炎病毒(HCV)属于黄病毒科肝炎病毒属,其基因组为单股正链RNA,由约 9.6*103核苷酸组成。据世界卫生组织统计,全球HCV的感染率约为2.8%,约1.85亿人感染HCV,每年因HCV感染导致的死亡病例约35万例。2006年我国血清流行病学调查显示,我国1~59岁人群抗-HCV流行率0.43%,在全球范围内属HCV低流行地区,即我国一般人群HCV感染者约560万,如加上高危人群和高发地区的HCV感染者,约1000万例。
在各种病毒性肝炎中,丙肝是我国常见的肝脏疾病之一,也是导致我国肝硬化和肝癌的主要原因之一。与家喻户晓的乙肝不同,丙肝就像一个沉默的杀手,善于“伪装”,长期潜伏损害肝脏,存在“三低”现象,即认知率低,诊断率低,治疗率低。
丙肝病毒主要通过血液传播、性接触和母婴传播。血液传播是目前最主要的传播方式,使用非一次性注射器和针头、未经严格消毒的牙科器械、内镜、侵袭性操作和针刺等也是经皮传播的重要途径。共用剃须刀、牙刷、纹身和穿耳环孔等也是丙肝病毒潜在的经血传播方式。与其他RNA病毒一样, 丙肝病毒基因组有很大的变异性, 可能会引起其分子生物学行为、感染性、临床致病性及对药物治疗的反应等诸方面的不同2-3 。
目前丙型肝炎的最大问题是随着丙肝药物的进展,其治疗的效果很好,SVR(持续病毒应答)可以达到95%以上, 但是真正接受抗病毒治疗的病人数非常少,都不到10%。要达到WHO提出的2030年丙肝新发感染人数减90%,治疗人数超过80%,死亡人数减少65%的目标任务仍然十分艰巨4,丙肝的早筛早诊刻不容缓。
丙型肝炎的检测
1.HCV抗体检验技术
HCV抗体检测技术是最早出现、研究和应用时间最久的HCV检测技术。自从1978年Shirachi et al首先报道用双向免疫扩散法在输血后肝炎患者急性期和恢复期血清中找到了丙型肝炎病毒特异性的抗原和抗体, 而后不少学者利用放射免疫(RIA)和酶联免疫(ELISA)等方法都曾找到了特异性的丙型肝炎病毒抗原和抗体5-6。1989年, Choo et al从大量有高度传染性的黑猩猩血浆中提取核酸, 经逆转录和分子克隆并进行筛选, 获得了部分HCV cDNA序列, 并表达重组抗原, 建立了特异性抗-HCV血清学的检测方法7-8。
HCV抗体检测技术历经十几年不断尝试、改良得到的有效检测方式,并进一步演变出ELISA、双抗原夹心、重组免疫印迹法(RIBA)、蛋白芯片检测法、间接酶联免疫吸附试验,免疫层析法以及现在主流的化学发光法等多种检测方式。
HCV抗体是由于人体免疫细胞对丙肝病毒感染所做出的反应而产生的。抗体在血液中循环而且经常性检测到存在。丙肝抗体对身体没有任何的保护作用,如果丙肝抗体呈阳性,并不一定就代表患有丙肝。是否患有丙肝的判断依据是血液中是否含有丙肝病毒,因此HCV抗体是反映HCV是否感染过的主要指标。
HCV抗体检测适用于高危人群筛查,也可用于HCV感染者的初筛。但抗-HCV阴转与否不能作为抗病毒疗效的指标。如一些透析、免疫功能缺陷和自身免疫性疾病患者可出现抗-HCV假阳性,免疫功能缺陷或合并HIV感染者可出现抗-HCV假阴性,急性丙型肝炎患者可因为抗-HCV检测处于窗口期出现抗-HCV阴性。因此,HCV RNA检测有助于确诊这些患者是否合并感染HCV。
2.HCV-RNA核酸扩增检测技术(NAT)
HCV-RNA是HCV复制的标志,HCV感染发生的14 天内即可检测发现HCV RNA,其可作为判断丙肝感染和丙肝治疗疗效的主要参考。HCV感染的早期确诊更依赖于灵敏的HCV-RNA定量检测。在不明原因的急性肝炎,为早期确诊时建议及时进行HCV-RNA定量检测。一般认为,有暴露史,实验室检测HCV-RNA阳性,并且出现HCV抗体的血清学转换,可确诊急性HCV感染。肝功能异常,转氨本酶10倍或以上升高,检测HCV-RNA阴性,HCV病毒学症持续超过6个月,认为是慢性感染。当前,NAT检测技术已经成为部分临床工作者使用的HCV感染确认途径使用。
HCV RNA检测包括定性和定量两种方法, 其基本原理就是逆转录聚合酶链反应(RT-PCR): 首先经逆转录酶作用,在特异性引物存在下,将HCV RNA逆转录为单链的cDNA, 再通过PCR将cDNA扩增。定性PCR的灵敏度高于定量PCR。因此定性PCR主要用于急慢性丙型肝炎诊断,而定量PCR则用于疗效监测。
近几年来随着实时荧光定量PCR技术的日趋成熟,HCV RNA定量检测的灵敏度逐渐提高,最低检测限可达12~15 IU/ml,接近甚至超过了定性检测的灵敏度,线性范围也在不断拓宽,且无需对PCR产物进行后续操作,减少了气溶胶的污染,基于这些优势,定量检测正逐渐取代定性检测用于献血员的筛查。与此同时,HCV RNA定量检测灵敏度的提高也会促进临床对抗病毒治疗过程中HCV RNA动力学变化与疗效之间的关系有更加深入的认识。
3.一种新的HCV检测方法: 血清中HCV核心抗原的检测
相比HCV 抗体检测,HCV核心抗原检测可将窗口期缩短1.5个月,且抗原检出仅比RNA晚2天(见图1);免疫功能受损或缺陷的群体如艾滋病患者、长期接受透析的肾病患者、器官移植患者或先天性免疫功能缺陷患者筛查HCV感染时,不宜选抗体检测,可选择RNA或抗原检测。
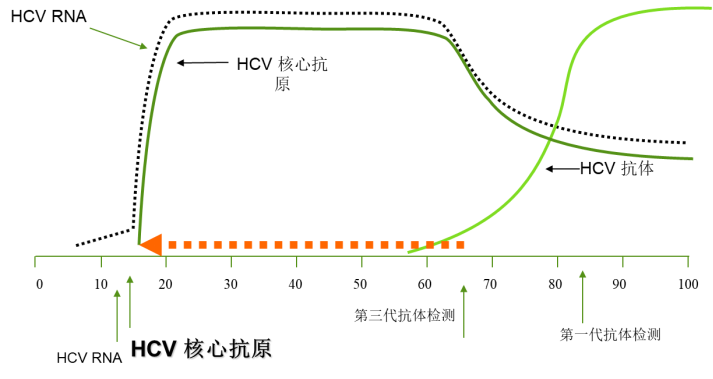
图1 HCV 核心抗原检测出现时间
自从1989年建立了丙肝病毒抗-HCV检测方法以来, 一些学者也曾经试图建立血清中HCV抗原的检测方法,但由于血液中HCV抗原含量太低,用常规方法无法检出。后来由于HCV单克隆抗体的研制成功, 已有国内外学者发表了肝组织及分泌物中HCV抗原检测成功的报道。
1996年Kashiwakuma et al9报道了用荧光酶免疫分析法(FEIA)检测血清中的HCV抗原, 该方法对重组核心抗原的检测灵敏度可达20 ng/L, 对血清中HCV核心抗原的检出与HCV RNA呈正相关, 在慢性丙肝患者中的检测率为92.3%(70/76); 1999年Aoyagi et al10建立了一种不需要特殊仪器设备的简单、高灵敏度的酶免分析法用于检测血清中的HCV核心抗原, 在该方法中先用三种去垢剂(TritonX-100, CHAPS和SDS)预处理被检标本, 即有效灭活标本中的抗核心抗原抗体, 检测结果不受血清样品中的抗凝剂或血液因子的影响, 125名健康人群和50例乙肝患者的HCV核心抗原检测均为阴性, 而73例抗-HCV阳性患者中HCV核心抗原检出率为78.1%(57/73), 与HCV RNA也有很好的相关性(r = 0.8, P<0.001)。
近几年随着化学发光法等免疫学检测技术的发展和成熟,灵敏、定量且适合自动化检测的HCV 核心抗原检测试剂已经研发成功,如雅培公司研发的ARCHITECT HCV Core Ag检测试剂11-12,使用该试剂对10份血清盘进行检测,结果表明,相比抗-HCV,HCV核心抗原检测可将窗口期缩短35.8天;在197份HCV RNA阳性血清盘标本中,196份(99.5%)HCV Ag阳性,193份(98%)为RNA阳性(Amplicor HCV Monitor 2.0),HCV核心抗原水平与RNA载量成正相关且两者呈相似的动力学变化;(见图2)。通过对5403份献血者、住院患者和非HCV相关疾病患者的标本进行检测,证明ARCHITECT HCV Core Ag的特异性可达99.8% 10。
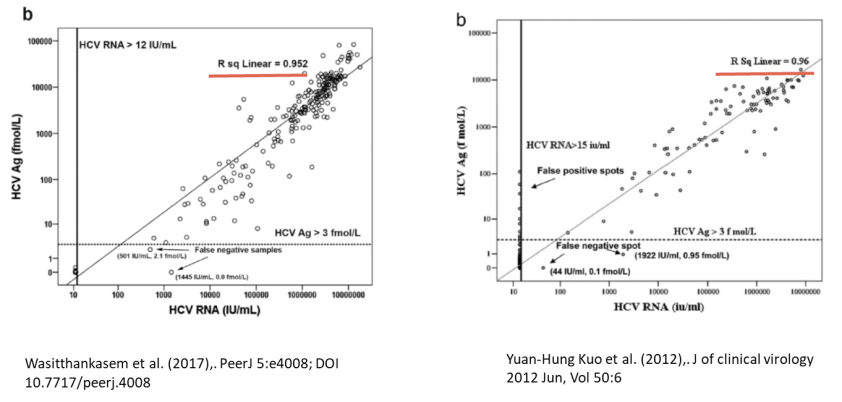
图2:Architect HCV Core Ag 与 HCV RNA 高度相关 目前几种常见的HCV核心抗原检测试剂及其原理13
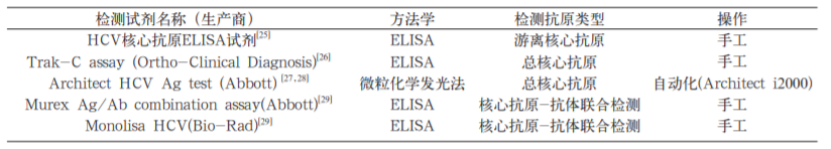
随着商用试剂盒的上市,HCV Core Ag越来越被广泛认可:日本将HCV core Ag纳入丙肝常规筛查流程14,爱尔兰将HCV core Ag(Abbott)纳入透析指南将其作为透析前以及透析过程中每3月必查项目15。众多文献也证实HCV core Ag检测的性能,如美国波士顿医疗中心的Freiman等学者系统检索了自1990 年至2016年3月31日的数据,总共纳入44项评估5项检测指标的研究,旨在评估更好的HCV检测方法。其中评估结果Abbott ARCHITECT HCV核心抗原检测的质量最高,并且可以达到与核酸检测(NAT)相仿的诊断准确性16。
随着DAA(直接抗病毒药物)的多种新药的陆续上市,丙型肝炎治疗新方案的不断探索,也为丙肝的消除奠定坚实的后盾。更好的应用丙型肝炎病毒抗原、抗体和RNA的联合检测已成为HCV感染诊断的主要指标, 扩大了检测范围, 缩短了窗口期, 有利于早期诊断, 同时对这些指标的出现与消退规律、及其与临床病理演变关系的追踪观察分析将对HCV感染情况、治疗方案的选择和预后判断等提供依据, 有更直接的意义。
在HCV抗体检测的基础上,更好的规范HCV RNA检测, 才能提高实验室检测结果的可信度; 同时作为HCV抗体检验的补充试验, 对于应用HCV核心抗原的检测方法, 可帮助提高对窗口期感染者的检出率,可潜在促进丙肝的检测及疾病防治。












